医药资讯
-
 Precede Biosciences获5700万美元A轮融资,利用血液加快精准药物的研发 Precede Biosciences是一家专注于精准医疗领域的生物科技公司。他们的目标是通过研究和开发新型技术和工具,利用个体血液样本来加快药物的研发过程。他们相信,通过深入了解个体血液中的生物标记物,可以更好地预测疾病的发展和药物治疗的效果,从而实现精准医疗。这笔5700万美元的融资将有助于Precede Biosciences进一步推动他们的研究和开发工作。他们计划利用这些资金进一步改进他们的技术和分析方法,提高其预测个体药物反应的准确性和精度。Precede Biosciences的创始人兼首席执行官表示,血液是一个非常重要的生物样本,其中包含了丰富的信息,可以用于预测疾病的发展和个体对药物的反应。通过深入研究血液中的生物标记物,他们希望能够帮助医生更好地为患者定制治疗方案,提高疗效,并减少不必要的药物副作用。另外,预计Precede Biosciences还将利用这笔融资加强公司的市场推广和扩大规模。公司计划招募更多的研发人员和专家,加快技术开发和临床研究进程,进一步提升公司的竞争力。总的来说,Precede Biosciences获得这笔5700万美元的A轮融资将对他们的研究和发展工作产生积极影响。通过利用血液来加快精准药物的研发,他们有望为患者提供更个性化和有效的治疗方案,以改善疾病的预后和生活质量。
Precede Biosciences获5700万美元A轮融资,利用血液加快精准药物的研发 Precede Biosciences是一家专注于精准医疗领域的生物科技公司。他们的目标是通过研究和开发新型技术和工具,利用个体血液样本来加快药物的研发过程。他们相信,通过深入了解个体血液中的生物标记物,可以更好地预测疾病的发展和药物治疗的效果,从而实现精准医疗。这笔5700万美元的融资将有助于Precede Biosciences进一步推动他们的研究和开发工作。他们计划利用这些资金进一步改进他们的技术和分析方法,提高其预测个体药物反应的准确性和精度。Precede Biosciences的创始人兼首席执行官表示,血液是一个非常重要的生物样本,其中包含了丰富的信息,可以用于预测疾病的发展和个体对药物的反应。通过深入研究血液中的生物标记物,他们希望能够帮助医生更好地为患者定制治疗方案,提高疗效,并减少不必要的药物副作用。另外,预计Precede Biosciences还将利用这笔融资加强公司的市场推广和扩大规模。公司计划招募更多的研发人员和专家,加快技术开发和临床研究进程,进一步提升公司的竞争力。总的来说,Precede Biosciences获得这笔5700万美元的A轮融资将对他们的研究和发展工作产生积极影响。通过利用血液来加快精准药物的研发,他们有望为患者提供更个性化和有效的治疗方案,以改善疾病的预后和生活质量。2023-10-10
-
 美机构:研发出能杀死所有实体癌瘤的药物AOH1996 美国顶级癌症治疗和研究机构希望城市(City of Hope)国家医疗中心周二发布公告称,在临床前研究中,该机构科学家开发出一种能杀死所有实体恶性肿瘤(癌瘤)的靶向化疗药物。 然而,中文互联网流传的“美机构研发出能杀死所有实体癌瘤的药物”这个消息,可信吗?凤凰网《CC情报局》请教了科普作家庄时利和、ZEALER,他们表示,这种药物我们每年都能见到几个到几十个,对于真实效果还需持谨慎态度。 仅在动物模型中杀死癌细胞,人体临床才可验证真实患者是否有效 公告里所提及的临床前研究,已经以论文的形式发表在《细胞化学生物学》期刊上。前文提及的这款药物(AOH1996),是一款用来遏制肿瘤细胞增殖的口服小分子PCNA(增殖细胞核抗原)抑制剂。背后的原理也很容易解释。增殖细胞核抗原在DNA复制和修复的过程中非常重要,这款药物特别针对增殖细胞核抗原的一个癌变形,这种蛋白质在所有扩展瘤的DNA复制和修复过程中起着关键作用。根据临床实验前研究的报告,研究人员在70多个癌细胞系和几组正常细胞中测试了AOH1996。这种研究性疗法阻止了带有损伤DNA的细胞在G2/M阶段分裂,并阻止了在S阶段复制错误的DNA。最终结果的结果是,AOH1996引发了癌细胞的死亡(或者叫凋亡),同时并没有中断健康干细胞的繁殖周期。 随着动物模型验证药物可行性后,AOH1996也已经进入Ⅰ期临床试验阶段,该阶段主要测试药物的安全性和推荐使用剂量等情况。根据美国临床试验资料库的数据显示,这个阶段的试验预期在明年3月底前结束。也就是说,大概在一年左右的时间里,我们就能看到这款药物在真实患者身上使用的数据(clinicaltrials.gov)。 进入临床试验阶段的药物中,最终只有约1/10可以获批上市,需谨慎观察 根据历史数据,所有候选药物能通过临床试验最终获批上市的概率(likelihood of approval,LOA)是9.6%,如果除开失败率最高的肿瘤类(oncology)药物临床试验的话,这个数字是11.9%。具体来说,Ⅰ期临床试验平均花费100~300万美金,成功率63.2%;Ⅱ期临床试验平均花费400~1200万美金,成功率30.7%;Ⅲ期临床试验平均花费3000~5000万美金,成功率58.1%;新药生产上市注册申请/生物制品许可申请(NDA/BLA)到最终获批,成功率85.3%。如果有Ⅳ期临床的话,平均还要相当于一次Ⅰ期临床试验的花费。 所以每10个有资格进入临床试验阶段的药物当中,最终只有1个可以获批上市。这还是抛开海量的在细胞实验或者动物试验阶段就折戟沉沙的药物,而今天媒体报道的这款药就还处于细胞实验阶段。希望城市(City of Hope)的临床试验确实非常多,癌症研究水平很强,但是还是要看后续这款药的临床试验结果,谨慎观察吧。对于肿瘤患者而言遵循指南治疗才是最重要的。
美机构:研发出能杀死所有实体癌瘤的药物AOH1996 美国顶级癌症治疗和研究机构希望城市(City of Hope)国家医疗中心周二发布公告称,在临床前研究中,该机构科学家开发出一种能杀死所有实体恶性肿瘤(癌瘤)的靶向化疗药物。 然而,中文互联网流传的“美机构研发出能杀死所有实体癌瘤的药物”这个消息,可信吗?凤凰网《CC情报局》请教了科普作家庄时利和、ZEALER,他们表示,这种药物我们每年都能见到几个到几十个,对于真实效果还需持谨慎态度。 仅在动物模型中杀死癌细胞,人体临床才可验证真实患者是否有效 公告里所提及的临床前研究,已经以论文的形式发表在《细胞化学生物学》期刊上。前文提及的这款药物(AOH1996),是一款用来遏制肿瘤细胞增殖的口服小分子PCNA(增殖细胞核抗原)抑制剂。背后的原理也很容易解释。增殖细胞核抗原在DNA复制和修复的过程中非常重要,这款药物特别针对增殖细胞核抗原的一个癌变形,这种蛋白质在所有扩展瘤的DNA复制和修复过程中起着关键作用。根据临床实验前研究的报告,研究人员在70多个癌细胞系和几组正常细胞中测试了AOH1996。这种研究性疗法阻止了带有损伤DNA的细胞在G2/M阶段分裂,并阻止了在S阶段复制错误的DNA。最终结果的结果是,AOH1996引发了癌细胞的死亡(或者叫凋亡),同时并没有中断健康干细胞的繁殖周期。 随着动物模型验证药物可行性后,AOH1996也已经进入Ⅰ期临床试验阶段,该阶段主要测试药物的安全性和推荐使用剂量等情况。根据美国临床试验资料库的数据显示,这个阶段的试验预期在明年3月底前结束。也就是说,大概在一年左右的时间里,我们就能看到这款药物在真实患者身上使用的数据(clinicaltrials.gov)。 进入临床试验阶段的药物中,最终只有约1/10可以获批上市,需谨慎观察 根据历史数据,所有候选药物能通过临床试验最终获批上市的概率(likelihood of approval,LOA)是9.6%,如果除开失败率最高的肿瘤类(oncology)药物临床试验的话,这个数字是11.9%。具体来说,Ⅰ期临床试验平均花费100~300万美金,成功率63.2%;Ⅱ期临床试验平均花费400~1200万美金,成功率30.7%;Ⅲ期临床试验平均花费3000~5000万美金,成功率58.1%;新药生产上市注册申请/生物制品许可申请(NDA/BLA)到最终获批,成功率85.3%。如果有Ⅳ期临床的话,平均还要相当于一次Ⅰ期临床试验的花费。 所以每10个有资格进入临床试验阶段的药物当中,最终只有1个可以获批上市。这还是抛开海量的在细胞实验或者动物试验阶段就折戟沉沙的药物,而今天媒体报道的这款药就还处于细胞实验阶段。希望城市(City of Hope)的临床试验确实非常多,癌症研究水平很强,但是还是要看后续这款药的临床试验结果,谨慎观察吧。对于肿瘤患者而言遵循指南治疗才是最重要的。2023-08-03
-
 AOH1996:能杀死所有实体恶性肿瘤(癌瘤)的靶向化疗药物 根据美国顶级癌症治疗和研究机构希望城市国家医疗中心的公告,他们的科学家在临床前研究中开发出一种能杀死所有实体恶性肿瘤(癌瘤)的靶向化疗药物。这个重要的突破意味着人们有望使用一种有效的治疗方法来对抗各种类型的癌症。 这款名为AOH1996的药物是一种口服小分子PCNA抑制剂,它的作用是阻止肿瘤细胞的增殖。在临床实验前的研究中,研究人员测试了AOH1996对70多个癌细胞系和几组正常细胞的影响。结果显示,这项研究性疗法能够阻止带有损伤DNA的细胞在G2/M阶段分裂,并且阻止在S阶段对DNA进行复制错误。这最终导致癌细胞的死亡或凋亡,而健康的干细胞的繁殖周期没有受到中断。 这个发现对于癌症治疗领域来说是一个重大的突破。传统的化疗药物常常会影响到正常细胞,导致一系列严重副作用,如恶心、呕吐和脱发等。然而,AOH1996的靶向作用使得它能够准确地攻击癌细胞,而不损伤健康细胞。这意味着患者在接受治疗时不会遭受严重的副作用,从而提高了治疗的耐受性和生活质量。 这项研究还在论文中详细介绍了AOH1996的作用机制和临床前研究结果。根据研究人员的观察,他们相信这种药物可能会成为未来癌症治疗的重要选择之一。然而,药物研发需要经历长期的临床试验和监测,以确保其安全性和有效性。希望城市国家医疗中心将继续进行进一步的研究,以验证这个突破性疗法的疗效,并最终将其带到临床环境中,造福于患者。 总的来说,AOH1996的开发是癌症治疗领域的一项重大突破。它的靶向作用能够精确攻击癌细胞,同时保护健康细胞,从而减少了副作用的发生。随着未来进一步的研究和发展,这种靶向化疗药物有望成为治疗各种类型癌症的重要工具,为患者带来新的希望和可能性。
AOH1996:能杀死所有实体恶性肿瘤(癌瘤)的靶向化疗药物 根据美国顶级癌症治疗和研究机构希望城市国家医疗中心的公告,他们的科学家在临床前研究中开发出一种能杀死所有实体恶性肿瘤(癌瘤)的靶向化疗药物。这个重要的突破意味着人们有望使用一种有效的治疗方法来对抗各种类型的癌症。 这款名为AOH1996的药物是一种口服小分子PCNA抑制剂,它的作用是阻止肿瘤细胞的增殖。在临床实验前的研究中,研究人员测试了AOH1996对70多个癌细胞系和几组正常细胞的影响。结果显示,这项研究性疗法能够阻止带有损伤DNA的细胞在G2/M阶段分裂,并且阻止在S阶段对DNA进行复制错误。这最终导致癌细胞的死亡或凋亡,而健康的干细胞的繁殖周期没有受到中断。 这个发现对于癌症治疗领域来说是一个重大的突破。传统的化疗药物常常会影响到正常细胞,导致一系列严重副作用,如恶心、呕吐和脱发等。然而,AOH1996的靶向作用使得它能够准确地攻击癌细胞,而不损伤健康细胞。这意味着患者在接受治疗时不会遭受严重的副作用,从而提高了治疗的耐受性和生活质量。 这项研究还在论文中详细介绍了AOH1996的作用机制和临床前研究结果。根据研究人员的观察,他们相信这种药物可能会成为未来癌症治疗的重要选择之一。然而,药物研发需要经历长期的临床试验和监测,以确保其安全性和有效性。希望城市国家医疗中心将继续进行进一步的研究,以验证这个突破性疗法的疗效,并最终将其带到临床环境中,造福于患者。 总的来说,AOH1996的开发是癌症治疗领域的一项重大突破。它的靶向作用能够精确攻击癌细胞,同时保护健康细胞,从而减少了副作用的发生。随着未来进一步的研究和发展,这种靶向化疗药物有望成为治疗各种类型癌症的重要工具,为患者带来新的希望和可能性。2023-08-03
-
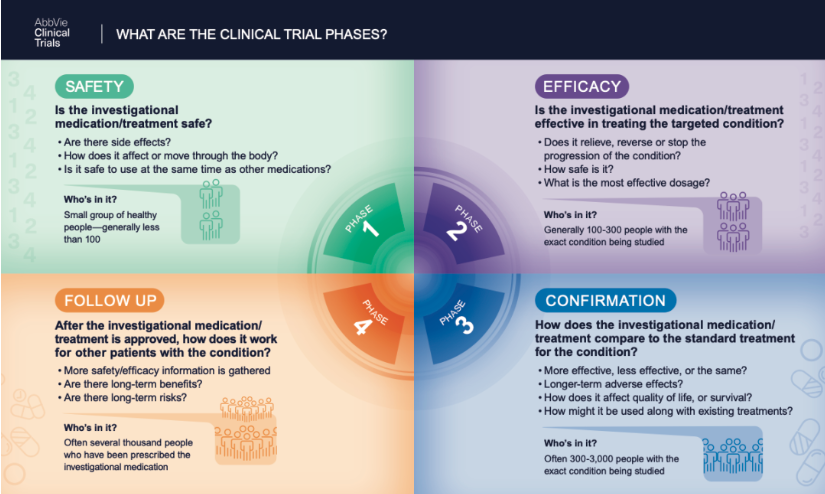 美国研发出能杀死所有恶性肿瘤的药物 癌症治疗取得历史性突破? 美国顶级癌症治疗和研究机构希望城市(City of Hope)国家医疗中心2日发布公告称,在临床前研究中,该机构科学家开发出一种能杀死所有实体恶性肿瘤(癌瘤)的靶向化疗药物。 这款药物被命名为AOH1996,是一款用来遏制肿瘤细胞增殖的口服小分子PCNA(增殖细胞核抗原)抑制剂。 根据介绍,这种研究性疗法阻止了带有损伤DNA的细胞在G2/M阶段分裂,并阻止了在S阶段复制错误的DNA。最终的结果是,AOH1996引发了癌细胞的死亡(或者叫凋亡),同时并没有中断健康干细胞的繁殖周期。 也就是说,药物“杀死”了癌细胞,但没有伤害正常细胞。 实际上,这个作用机制从医学上来说并不是最新发明,现在常用的化疗药基本都是靶向细胞周期干预肿瘤细胞复制的。但是不管化疗药怎么组合,多数情况下,肿瘤细胞总是能找到办法逃逸。这也是肿瘤治疗一直以来难以有所突破的症结所在。 如今,这款AOH1996宣称在这个机制中找到了新的靶点,即PCNA,并在试验中取得很好的效果。临床前研究已经以论文的形式发表在《细胞化学生物学》期刊上。 但是,这能否就让靶向DNA复制或者细胞周期的抗肿瘤药物实现革命性变化,还需要更多数据和试验,以及时间。 目前,这个药物仍在I期临床试验阶段,尚在探索药物安全性。根据美国临床试验资料库的数据显示,这个阶段的试验预期在明年3月底前结束。也就是说,大概在一年左右的时间里,我们就能看到这款药物在真实患者身上使用的数据。 这里可以简单说一下药物上市前要走的漫长且严谨的流程: I期临床试验主要是进行初步的临床药理学研究和人体用药的安全性评价,一般要求20-30例患者。 II期临床试验是对药物的治疗作用进行初步评价,要有超过100例患者参与。 III期临床试验是对II期的再次确认,要求超过300例患者。 这整个过程一般都需要三年甚至更久的时间。而且,过了III期试验后,才可以申请上市,申请上市又需要一定的审批时间。即便上市,药物还需要进行IV期临床试验,样本量要超过2000例,以考察药物的疗效及不良反应。 所以,正如网友所说,虽然对AOH1996有所期待,但现在谈“成功”还为时尚早,“就像开场5分钟就开香槟庆祝”。 此外,也有专业分析对其试验的具体细节持有保留意见。例如,根据临床试验前研究的报告,研究人员是在70多个癌细胞系和几组正常细胞中测试的AOH1996。 肿瘤细胞的细胞系是从某些病人身上分裂出来的一些肿瘤细胞在体外扩增,全世界的研究人员都用这些细胞做研究。但是体外细胞系和体内的癌细胞,不管在所处的周边血管环境还是与其他成分间的相互作用等方面,都有很大的差别。“如果想体外模型抗肿瘤,只需要把这些细胞泡在60度热水里就能轻松杀死它们”,显然,真实的病症治疗却复杂太多。 人类与疾病的斗争向来都是充满不确定性的,我们都很希望早日赢得这场战争的胜利,减少AOH1996药物名字里所藏的那个遗憾——一个1996年出生、9岁死于神经母细胞瘤的女孩Anna Olivia Healy,她的名字缩写加出生年份就是这个药物的代号。
美国研发出能杀死所有恶性肿瘤的药物 癌症治疗取得历史性突破? 美国顶级癌症治疗和研究机构希望城市(City of Hope)国家医疗中心2日发布公告称,在临床前研究中,该机构科学家开发出一种能杀死所有实体恶性肿瘤(癌瘤)的靶向化疗药物。 这款药物被命名为AOH1996,是一款用来遏制肿瘤细胞增殖的口服小分子PCNA(增殖细胞核抗原)抑制剂。 根据介绍,这种研究性疗法阻止了带有损伤DNA的细胞在G2/M阶段分裂,并阻止了在S阶段复制错误的DNA。最终的结果是,AOH1996引发了癌细胞的死亡(或者叫凋亡),同时并没有中断健康干细胞的繁殖周期。 也就是说,药物“杀死”了癌细胞,但没有伤害正常细胞。 实际上,这个作用机制从医学上来说并不是最新发明,现在常用的化疗药基本都是靶向细胞周期干预肿瘤细胞复制的。但是不管化疗药怎么组合,多数情况下,肿瘤细胞总是能找到办法逃逸。这也是肿瘤治疗一直以来难以有所突破的症结所在。 如今,这款AOH1996宣称在这个机制中找到了新的靶点,即PCNA,并在试验中取得很好的效果。临床前研究已经以论文的形式发表在《细胞化学生物学》期刊上。 但是,这能否就让靶向DNA复制或者细胞周期的抗肿瘤药物实现革命性变化,还需要更多数据和试验,以及时间。 目前,这个药物仍在I期临床试验阶段,尚在探索药物安全性。根据美国临床试验资料库的数据显示,这个阶段的试验预期在明年3月底前结束。也就是说,大概在一年左右的时间里,我们就能看到这款药物在真实患者身上使用的数据。 这里可以简单说一下药物上市前要走的漫长且严谨的流程: I期临床试验主要是进行初步的临床药理学研究和人体用药的安全性评价,一般要求20-30例患者。 II期临床试验是对药物的治疗作用进行初步评价,要有超过100例患者参与。 III期临床试验是对II期的再次确认,要求超过300例患者。 这整个过程一般都需要三年甚至更久的时间。而且,过了III期试验后,才可以申请上市,申请上市又需要一定的审批时间。即便上市,药物还需要进行IV期临床试验,样本量要超过2000例,以考察药物的疗效及不良反应。 所以,正如网友所说,虽然对AOH1996有所期待,但现在谈“成功”还为时尚早,“就像开场5分钟就开香槟庆祝”。 此外,也有专业分析对其试验的具体细节持有保留意见。例如,根据临床试验前研究的报告,研究人员是在70多个癌细胞系和几组正常细胞中测试的AOH1996。 肿瘤细胞的细胞系是从某些病人身上分裂出来的一些肿瘤细胞在体外扩增,全世界的研究人员都用这些细胞做研究。但是体外细胞系和体内的癌细胞,不管在所处的周边血管环境还是与其他成分间的相互作用等方面,都有很大的差别。“如果想体外模型抗肿瘤,只需要把这些细胞泡在60度热水里就能轻松杀死它们”,显然,真实的病症治疗却复杂太多。 人类与疾病的斗争向来都是充满不确定性的,我们都很希望早日赢得这场战争的胜利,减少AOH1996药物名字里所藏的那个遗憾——一个1996年出生、9岁死于神经母细胞瘤的女孩Anna Olivia Healy,她的名字缩写加出生年份就是这个药物的代号。2023-05-17
-
 纵膈肿瘤 纵膈是指胸腔内的上方区域,由各种结构如支气管、食管、心脏、主动脉等组成,因此纵膈肿瘤可以来自于上述结构中的任何一个或多个。其中最常见的纵膈肿瘤包括甲状腺肿瘤、胸腺肿瘤、淋巴瘤、神经肿瘤等。下面,我们就来一起了解一下纵膈肿瘤吧。 首先,纵膈肿瘤的症状与位置有关。对于靠前的纵膈肿瘤,常常出现咳嗽、呼吸困难、胸痛等症状,当瘤体增大时可能会影响食管,导致吞咽不适或者进食呛咳。而对于靠后的纵膈肿瘤,由于其位置较深,可能不会出现明显的症状,但是当瘤体增大至压迫邻近器官时,仍然会产生相应的症状,例如背痛、手臂无力、声音嘶哑等。 其次,纵膈肿瘤的治疗方式也因肿瘤的类型、大小和位置而有所不同。对于较小的纵膈肿瘤,可以采取手术切除的方式进行治疗,但是对于部分位置较深或较大的肿瘤,可能需要辅助性放疗或化疗。在具体的治疗方案中,也需要结合患者的年龄、身体状况、生活习惯等因素综合考虑,以制定最合适的治疗方案。 最后,对于纵膈肿瘤的预防,我们也需要注意预防患病的因素。生活中,可以通过适当运动、饮食清淡、保持心情愉悦等方式来加强自身免疫力,降低患病的风险。同时,在生活中也要注意避免吸烟、酗酒等不良习惯,减少暴露于工业污染、尘埃等有害环境中的时间,以避免引发纵膈肿瘤的风险。 综上所述,纵膈肿瘤作为一种比较常见的肿瘤疾病,对于我们的身体健康也会产生不良影响。因此,我们在日常生活中要多加注意自身的身体健康,并及时进行体检,以便早发现、早治疗,保护我们的身体健康。
纵膈肿瘤 纵膈是指胸腔内的上方区域,由各种结构如支气管、食管、心脏、主动脉等组成,因此纵膈肿瘤可以来自于上述结构中的任何一个或多个。其中最常见的纵膈肿瘤包括甲状腺肿瘤、胸腺肿瘤、淋巴瘤、神经肿瘤等。下面,我们就来一起了解一下纵膈肿瘤吧。 首先,纵膈肿瘤的症状与位置有关。对于靠前的纵膈肿瘤,常常出现咳嗽、呼吸困难、胸痛等症状,当瘤体增大时可能会影响食管,导致吞咽不适或者进食呛咳。而对于靠后的纵膈肿瘤,由于其位置较深,可能不会出现明显的症状,但是当瘤体增大至压迫邻近器官时,仍然会产生相应的症状,例如背痛、手臂无力、声音嘶哑等。 其次,纵膈肿瘤的治疗方式也因肿瘤的类型、大小和位置而有所不同。对于较小的纵膈肿瘤,可以采取手术切除的方式进行治疗,但是对于部分位置较深或较大的肿瘤,可能需要辅助性放疗或化疗。在具体的治疗方案中,也需要结合患者的年龄、身体状况、生活习惯等因素综合考虑,以制定最合适的治疗方案。 最后,对于纵膈肿瘤的预防,我们也需要注意预防患病的因素。生活中,可以通过适当运动、饮食清淡、保持心情愉悦等方式来加强自身免疫力,降低患病的风险。同时,在生活中也要注意避免吸烟、酗酒等不良习惯,减少暴露于工业污染、尘埃等有害环境中的时间,以避免引发纵膈肿瘤的风险。 综上所述,纵膈肿瘤作为一种比较常见的肿瘤疾病,对于我们的身体健康也会产生不良影响。因此,我们在日常生活中要多加注意自身的身体健康,并及时进行体检,以便早发现、早治疗,保护我们的身体健康。2023-05-05
-
 肿瘤转移 肿瘤转移,即癌症的远处转移,是肿瘤最为危险的特征之一,也是治疗肿瘤时需要考虑到的重要问题。而癌细胞扩散和转移的机制,一直是癌症研究的重点。 癌症的转移是指癌症细胞从原发部位穿过周围组织、进入血管或淋巴管,随后通过血流或淋巴流到达身体的其他部位,然后在新的器官和组织中生长复制,从而形成远处的转移灶。 为什么癌症会出现转移呢?因为癌症细胞是异常细胞,它们分裂比正常细胞快,且无法停止,会不断蔓延,形成癌症肿块。随着时间推移,恶性肿瘤会继续生长侵入周围的血管和淋巴管,从而迅速转移到身体其他部位。 肿瘤转移是癌症的严重并发症,也是预后差的表现。肿瘤转移后,癌症的治疗难度大大增加,治疗方案需要更加复杂、全面,治疗效果难以预测。此外,癌症转移也会给肿瘤患者带来大量痛苦,影响生活质量,甚至威胁生命。 那么,肿瘤转移具体发生在哪些器官和部位呢?一般来说,癌症转移是可以发生在全身的。根据部位不同,可以分为淋巴转移和血行转移两种类型。 淋巴转移是指肿瘤细胞从原发灶扩散到淋巴系统,从而到达淋巴结。在这个过程中,肿瘤细胞可以在淋巴管内或淋巴结中形成新的转移灶。淋巴转移是癌症扩散的一个主要途径,例如乳腺癌常常通过淋巴转移扩散到腋窝淋巴结。 血行转移是指肿瘤细胞通过血管系统到达身体的其他部位,也是癌症扩散的重要途径。肿瘤细胞可以通过血管内皮细胞间隙浸润,甚至直接穿过血管壁进入血管。一旦进入血流,肿瘤细胞就可以在循环系统中远距离转移。血行转移是许多癌症形成多器官转移灶的主要原因之一,例如肺癌常常通过血行转移到达骨、肝、脑等器官。 总之,肿瘤转移是癌症严重的并发症,给患者的康复带来极大的困难。因此,早期发现肿瘤、科学治疗是预防癌症转移的关键。同时,癌症患者需要积极调整心态,细心照顾自己,早日摆脱癌症转移的困扰。
肿瘤转移 肿瘤转移,即癌症的远处转移,是肿瘤最为危险的特征之一,也是治疗肿瘤时需要考虑到的重要问题。而癌细胞扩散和转移的机制,一直是癌症研究的重点。 癌症的转移是指癌症细胞从原发部位穿过周围组织、进入血管或淋巴管,随后通过血流或淋巴流到达身体的其他部位,然后在新的器官和组织中生长复制,从而形成远处的转移灶。 为什么癌症会出现转移呢?因为癌症细胞是异常细胞,它们分裂比正常细胞快,且无法停止,会不断蔓延,形成癌症肿块。随着时间推移,恶性肿瘤会继续生长侵入周围的血管和淋巴管,从而迅速转移到身体其他部位。 肿瘤转移是癌症的严重并发症,也是预后差的表现。肿瘤转移后,癌症的治疗难度大大增加,治疗方案需要更加复杂、全面,治疗效果难以预测。此外,癌症转移也会给肿瘤患者带来大量痛苦,影响生活质量,甚至威胁生命。 那么,肿瘤转移具体发生在哪些器官和部位呢?一般来说,癌症转移是可以发生在全身的。根据部位不同,可以分为淋巴转移和血行转移两种类型。 淋巴转移是指肿瘤细胞从原发灶扩散到淋巴系统,从而到达淋巴结。在这个过程中,肿瘤细胞可以在淋巴管内或淋巴结中形成新的转移灶。淋巴转移是癌症扩散的一个主要途径,例如乳腺癌常常通过淋巴转移扩散到腋窝淋巴结。 血行转移是指肿瘤细胞通过血管系统到达身体的其他部位,也是癌症扩散的重要途径。肿瘤细胞可以通过血管内皮细胞间隙浸润,甚至直接穿过血管壁进入血管。一旦进入血流,肿瘤细胞就可以在循环系统中远距离转移。血行转移是许多癌症形成多器官转移灶的主要原因之一,例如肺癌常常通过血行转移到达骨、肝、脑等器官。 总之,肿瘤转移是癌症严重的并发症,给患者的康复带来极大的困难。因此,早期发现肿瘤、科学治疗是预防癌症转移的关键。同时,癌症患者需要积极调整心态,细心照顾自己,早日摆脱癌症转移的困扰。2023-05-05
-
 肿瘤治疗 随着生活水平的不断提高,人们的生活方式和饮食习惯也越来越趋向于现代化和高脂高糖的方向,这使得肿瘤患者的数量急剧上升。肿瘤是一种严重的疾病,给患者带来了极大的痛苦和折磨,也威胁着他们的生命安全。针对不同类型的肿瘤,医生们采用了多种方式来进行治疗,其中包括化疗、放疗、手术等。下面就让我们一起来探讨一下肿瘤治疗的相关问题。 首先,化疗是指通过给患者注射一定剂量的化学药物,以杀死肿瘤细胞的治疗方法。化疗可根据不同的肿瘤类型和患者情况采用不同的方案,一般情况下,时间会比较长,需要患者坚持长时间治疗,同时需要注意身体的营养和调整体内的药物浓度。同时,化疗可能会对患者产生很大的副作用,如恶心、呕吐、脱发等,需要患者在治疗期间不断地调整自己的心态。 其次,放疗是指利用射线或其他类型的物质对肿瘤细胞进行杀死,同时保护周围正常细胞的治疗方法。放疗可以单独使用,也可以和化疗合并使用。放疗通常需要较短的时间,但是在治疗期间也可能会引起一定的副作用,如皮肤受损、口腔溃疡等。因此,在放疗前后,患者需要适当地保护自己的身体,保持营养充足和避免生活上的摩擦。 最后,手术是指通过外科手术的方式,将肿瘤组织切除的治疗方法。手术对于早期发现的肿瘤其治愈率很高,但对于晚期患者,手术不一定能切除全体肿瘤组织。因此,在手术前,需要医生对患者的情况进行综合评估,在尽量保证治愈率的前提下,减少身体的创伤和手术后的恢复时间。 综上所述,对于肿瘤治疗来说,针对不同的患者和肿瘤类型,不同的治疗方法各有优缺点。虽然治疗方法各有不同,但是重要的是患者需要在治疗期间保持良好的心态,同时加强身体锻炼和保持营养充足,这样才能更好地战胜肿瘤。相信在医学科技的不断进步和发展下,我们会更好地治疗肿瘤,也能使患者在治疗期间不断地找到希望和力量。
肿瘤治疗 随着生活水平的不断提高,人们的生活方式和饮食习惯也越来越趋向于现代化和高脂高糖的方向,这使得肿瘤患者的数量急剧上升。肿瘤是一种严重的疾病,给患者带来了极大的痛苦和折磨,也威胁着他们的生命安全。针对不同类型的肿瘤,医生们采用了多种方式来进行治疗,其中包括化疗、放疗、手术等。下面就让我们一起来探讨一下肿瘤治疗的相关问题。 首先,化疗是指通过给患者注射一定剂量的化学药物,以杀死肿瘤细胞的治疗方法。化疗可根据不同的肿瘤类型和患者情况采用不同的方案,一般情况下,时间会比较长,需要患者坚持长时间治疗,同时需要注意身体的营养和调整体内的药物浓度。同时,化疗可能会对患者产生很大的副作用,如恶心、呕吐、脱发等,需要患者在治疗期间不断地调整自己的心态。 其次,放疗是指利用射线或其他类型的物质对肿瘤细胞进行杀死,同时保护周围正常细胞的治疗方法。放疗可以单独使用,也可以和化疗合并使用。放疗通常需要较短的时间,但是在治疗期间也可能会引起一定的副作用,如皮肤受损、口腔溃疡等。因此,在放疗前后,患者需要适当地保护自己的身体,保持营养充足和避免生活上的摩擦。 最后,手术是指通过外科手术的方式,将肿瘤组织切除的治疗方法。手术对于早期发现的肿瘤其治愈率很高,但对于晚期患者,手术不一定能切除全体肿瘤组织。因此,在手术前,需要医生对患者的情况进行综合评估,在尽量保证治愈率的前提下,减少身体的创伤和手术后的恢复时间。 综上所述,对于肿瘤治疗来说,针对不同的患者和肿瘤类型,不同的治疗方法各有优缺点。虽然治疗方法各有不同,但是重要的是患者需要在治疗期间保持良好的心态,同时加强身体锻炼和保持营养充足,这样才能更好地战胜肿瘤。相信在医学科技的不断进步和发展下,我们会更好地治疗肿瘤,也能使患者在治疗期间不断地找到希望和力量。2023-05-05
-
 肿瘤科 肿瘤科是研究癌症的发病原因、病理变化、治疗方法以及预防措施等方面的一门学科。自从肿瘤的发现以来,肿瘤科医生一直致力于研究肿瘤的生长、分化、转移和治疗等方面的问题。在现代医学中,肿瘤科在较短的时间内发展至今,成为了现代医学的一大支柱之一。 肿瘤是人类至今未能完全解决的一大难题,虽然医学的发展越来越快,但是对肿瘤完全治愈的方法还没有找到。但是肿瘤科医生在肿瘤的治疗上已经有了很多进展,能够通过手术、放射治疗以及化疗等方法来控制病情发展,甚至有一些疾病可以通过治疗入院和化疗彻底治愈。 肿瘤科医生在日常工作中不仅需要具备医学专业知识,还需要有较高的人际沟通能力和心理疏导能力。在与病人沟通时,肿瘤科医生不但要为患者清楚的解释病情和治疗方案,并且能够给予患者温暖的关怀和安慰,缓解患者的痛苦和恐惧。其次,在治疗过程中,由于治疗周期较长,患者常常会出现身心上的极度疲乏和退化,肿瘤科医生需要及时关注病人的身心情况,给患者及家属以宣泄情绪的机会,缓解其情感压力。 另一方面,为了更有效地治疗肿瘤,肿瘤科医生需要对肿瘤细胞进行充分的研究,探讨肿瘤治疗的新方法及新技术。科技的发展为肿瘤治疗带来了新的希望,例如免疫治疗和基因治疗等先进技术成为了目前研究重点。同时,医生们始终坚持肿瘤防治的理念,通过宣传肿瘤防治的知识,提高人们对疾病的认识,降低疾病发生的概率,预防肿瘤的发生。 总之,对于肿瘤科医生来说,既需要科学严谨地治疗疾病,又需要充分顾及患者的身体与心理健康,这是医者的天职。肿瘤科医生是在解决人类千古难题的征程中所走过的重要一步,将医学科技和人文情操完美结合,成为了医学领域的不朽之人。
肿瘤科 肿瘤科是研究癌症的发病原因、病理变化、治疗方法以及预防措施等方面的一门学科。自从肿瘤的发现以来,肿瘤科医生一直致力于研究肿瘤的生长、分化、转移和治疗等方面的问题。在现代医学中,肿瘤科在较短的时间内发展至今,成为了现代医学的一大支柱之一。 肿瘤是人类至今未能完全解决的一大难题,虽然医学的发展越来越快,但是对肿瘤完全治愈的方法还没有找到。但是肿瘤科医生在肿瘤的治疗上已经有了很多进展,能够通过手术、放射治疗以及化疗等方法来控制病情发展,甚至有一些疾病可以通过治疗入院和化疗彻底治愈。 肿瘤科医生在日常工作中不仅需要具备医学专业知识,还需要有较高的人际沟通能力和心理疏导能力。在与病人沟通时,肿瘤科医生不但要为患者清楚的解释病情和治疗方案,并且能够给予患者温暖的关怀和安慰,缓解患者的痛苦和恐惧。其次,在治疗过程中,由于治疗周期较长,患者常常会出现身心上的极度疲乏和退化,肿瘤科医生需要及时关注病人的身心情况,给患者及家属以宣泄情绪的机会,缓解其情感压力。 另一方面,为了更有效地治疗肿瘤,肿瘤科医生需要对肿瘤细胞进行充分的研究,探讨肿瘤治疗的新方法及新技术。科技的发展为肿瘤治疗带来了新的希望,例如免疫治疗和基因治疗等先进技术成为了目前研究重点。同时,医生们始终坚持肿瘤防治的理念,通过宣传肿瘤防治的知识,提高人们对疾病的认识,降低疾病发生的概率,预防肿瘤的发生。 总之,对于肿瘤科医生来说,既需要科学严谨地治疗疾病,又需要充分顾及患者的身体与心理健康,这是医者的天职。肿瘤科医生是在解决人类千古难题的征程中所走过的重要一步,将医学科技和人文情操完美结合,成为了医学领域的不朽之人。2023-05-05
-
 中医治疗肿瘤 中医治疗肿瘤,是中医学研究领域的重点之一。与西医的化疗、手术、放疗等传统治疗方式相比,中医治疗肿瘤的方法更为温和、自然,且副作用小,能够显著提高患者的生活质量。 中医治疗肿瘤的方法多样,常用的治疗手段包括中药汤剂、针灸、推拿、气功等。中药汤剂是中医治疗肿瘤的主要手段之一,很多患者都用中药治疗肿瘤获得了良好的效果。中药治疗肿瘤的主要原理是调节机体内环境,增强机体的免疫力,攻击肿瘤细胞。针灸和推拿在中医治疗肿瘤方面也有较为广泛的应用。针灸的主要目的是通过调节人体气机,达到消肿、止痛、扶正抗癌的目的。推拿则是通过按摩某些穴位,刺激患处神经,从而达到缓解病情、促进血液循环的目的。 中医对肿瘤的防治一直处于领先地位。中医治疗肿瘤以调节气血为主,辅以补肾固本和提高机体免疫力的方法,从而增加机体的抵御能力。中医治疗肿瘤的效果因人而异,一般需要在较长时间内持续地进行,以达到较好的治疗效果。如果治疗方法得当,肿瘤可以得到显著的缩小或消除,达到甚至能治愈的效果。而且治疗过程中无创伤,不影响患者正常活动,重要的是中医治疗肿瘤副作用小,患者能够更好地承受治疗。 虽然中医治疗肿瘤的方法多样,但是也需要具有一定的技术及治疗经验的中医来进行治疗。因为中医治疗肿瘤,需要对病情进行全面、个性化的判断,根据病人的具体情况制定出有针对性的治疗方案,方案的制定及调整需要根据患者不断变化的病情进行调整。因此,在选择中医治疗肿瘤的时候,需要更加严谨、专业,找有相应资质的、有一定治疗经验的医生进行治疗。 总之,中医治疗肿瘤具有方法简单、副作用小、调节气血、提高机体免疫力等优点。但是,我们也必须看到,中医治疗肿瘤只是一个治疗手段,他并不是完全取代西医,也无法完全替代西医。在治疗中,中西医结合或是综合治疗是一个更好的选择。相信在科研人员和医生们的共同努力下,中医治疗肿瘤会不断升级创新,为中国的医疗事业带来更大的贡献。
中医治疗肿瘤 中医治疗肿瘤,是中医学研究领域的重点之一。与西医的化疗、手术、放疗等传统治疗方式相比,中医治疗肿瘤的方法更为温和、自然,且副作用小,能够显著提高患者的生活质量。 中医治疗肿瘤的方法多样,常用的治疗手段包括中药汤剂、针灸、推拿、气功等。中药汤剂是中医治疗肿瘤的主要手段之一,很多患者都用中药治疗肿瘤获得了良好的效果。中药治疗肿瘤的主要原理是调节机体内环境,增强机体的免疫力,攻击肿瘤细胞。针灸和推拿在中医治疗肿瘤方面也有较为广泛的应用。针灸的主要目的是通过调节人体气机,达到消肿、止痛、扶正抗癌的目的。推拿则是通过按摩某些穴位,刺激患处神经,从而达到缓解病情、促进血液循环的目的。 中医对肿瘤的防治一直处于领先地位。中医治疗肿瘤以调节气血为主,辅以补肾固本和提高机体免疫力的方法,从而增加机体的抵御能力。中医治疗肿瘤的效果因人而异,一般需要在较长时间内持续地进行,以达到较好的治疗效果。如果治疗方法得当,肿瘤可以得到显著的缩小或消除,达到甚至能治愈的效果。而且治疗过程中无创伤,不影响患者正常活动,重要的是中医治疗肿瘤副作用小,患者能够更好地承受治疗。 虽然中医治疗肿瘤的方法多样,但是也需要具有一定的技术及治疗经验的中医来进行治疗。因为中医治疗肿瘤,需要对病情进行全面、个性化的判断,根据病人的具体情况制定出有针对性的治疗方案,方案的制定及调整需要根据患者不断变化的病情进行调整。因此,在选择中医治疗肿瘤的时候,需要更加严谨、专业,找有相应资质的、有一定治疗经验的医生进行治疗。 总之,中医治疗肿瘤具有方法简单、副作用小、调节气血、提高机体免疫力等优点。但是,我们也必须看到,中医治疗肿瘤只是一个治疗手段,他并不是完全取代西医,也无法完全替代西医。在治疗中,中西医结合或是综合治疗是一个更好的选择。相信在科研人员和医生们的共同努力下,中医治疗肿瘤会不断升级创新,为中国的医疗事业带来更大的贡献。2023-05-05
-
 胰腺肿瘤 胰腺肿瘤是近年来越来越受到关注的一种疾病,据统计每年全球有超过46,000名患者死于这种肿瘤。胰腺是一个重要的器官,它负责分泌胰液和激素,而胰腺肿瘤则会干扰胰腺的功能,造成多种健康问题。本文将简要介绍胰腺肿瘤的类型、症状和治疗方案。 胰腺肿瘤通常分为良性和恶性两种,其中恶性肿瘤更加常见。胰腺癌是其中最为严重的一种,它的病因不明确,但是有一些因素被认为可能会增加患癌症的风险,比如:吸烟、长期饮酒、胰腺炎、遗传基因等。此外,还有一些罕见的胰腺肿瘤,如神经内分泌肿瘤和胰腺囊性肿瘤。 胰腺肿瘤通常是不易被察觉的,因为它们的症状很容易被误解为其他身体问题。但通常情况下,当肿瘤增大时,患者会出现压迫性疼痛、黄疸、恶心、呕吐等症状。有些人还可能会感受到胰腺区域的肿块。 对于诊断胰腺肿瘤,医生通常会建议进行影像检查和病理检查。其中,CT、MRI、超声等成像技术可以更好地确定肿瘤的大小和位置,而通过活检、手术切除等方法可以确定肿瘤是良性还是恶性。 治疗方案则取决于肿瘤的类型、大小和位置等因素。对于小且良性的肿瘤,通常并不需要治疗或者只需要随访治疗。而大的、恶性的肿瘤则需要尽早治疗,通常采用的是手术切除、放疗和化疗等方法。 总的来说,胰腺肿瘤是一种不容忽视的疾病。早期的诊断和治疗可以有效提高患者的生存率和生活质量。因此,我们应该保持健康的生活习惯、积极接受常规检查以及尽早发现和治疗可能存在的健康问题,以保证自己的健康和家庭的幸福。
胰腺肿瘤 胰腺肿瘤是近年来越来越受到关注的一种疾病,据统计每年全球有超过46,000名患者死于这种肿瘤。胰腺是一个重要的器官,它负责分泌胰液和激素,而胰腺肿瘤则会干扰胰腺的功能,造成多种健康问题。本文将简要介绍胰腺肿瘤的类型、症状和治疗方案。 胰腺肿瘤通常分为良性和恶性两种,其中恶性肿瘤更加常见。胰腺癌是其中最为严重的一种,它的病因不明确,但是有一些因素被认为可能会增加患癌症的风险,比如:吸烟、长期饮酒、胰腺炎、遗传基因等。此外,还有一些罕见的胰腺肿瘤,如神经内分泌肿瘤和胰腺囊性肿瘤。 胰腺肿瘤通常是不易被察觉的,因为它们的症状很容易被误解为其他身体问题。但通常情况下,当肿瘤增大时,患者会出现压迫性疼痛、黄疸、恶心、呕吐等症状。有些人还可能会感受到胰腺区域的肿块。 对于诊断胰腺肿瘤,医生通常会建议进行影像检查和病理检查。其中,CT、MRI、超声等成像技术可以更好地确定肿瘤的大小和位置,而通过活检、手术切除等方法可以确定肿瘤是良性还是恶性。 治疗方案则取决于肿瘤的类型、大小和位置等因素。对于小且良性的肿瘤,通常并不需要治疗或者只需要随访治疗。而大的、恶性的肿瘤则需要尽早治疗,通常采用的是手术切除、放疗和化疗等方法。 总的来说,胰腺肿瘤是一种不容忽视的疾病。早期的诊断和治疗可以有效提高患者的生存率和生活质量。因此,我们应该保持健康的生活习惯、积极接受常规检查以及尽早发现和治疗可能存在的健康问题,以保证自己的健康和家庭的幸福。2023-05-05
大家都在看